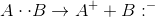1.
Struktur
Lewis berikut ini:

adalah representasi
dari
A.
NO2-
B.
NO2+
C.
NO2
D.
NO2+
dan NO2-
E.
NO2,
NO2+ dan NO2-
Jawab: B
elektron valensi
total NO2 = 5 + 2 x 6 = 17.
Elektron valensi
total pada sruktur lewis pada soal di atas adalah 16, sehingga muatan formal
senyawa pada struktur lewis di atas adalah 17-16 = +1.
Sehingga senyawa
tersebut adalah NO2+.
2.
Diantara
senyawa alkana berikut ini yang mempunyai interaksi van der Waals paling tinggi
adalah
A.
CH3CH2CH2CH2CH2CH3
B.
CH3CH2CH3
C.
CH3CH2C(CH2)4CH3
D.
CH3CH2CH2CH3
E.
CH3(CH2)3CH3
Jawab: C
Interaksi van der
Waals dipengaruhi oleh berat molekul. Semakin tinggi berat molekul semakin
tinggi pula interaksi van der Waals.
3.
Jika
NaBr larut dalam air, maka jenis gaya antar molekul yang harus diputuskan
adalah
A.
Gaya
ion-ion
B.
Ikatan-Hidrogen
C.
Gaya
ion-dipol
D.
Gaya
ion-ion dan ikatan hidrogen
E.
Dipol-dipol
Jawab:D
Ketika NaBr larut
dalam air, maka ion Na+ dan Br- masing-masing akan
tersolvasi oleh molekul air. Pada keadaan ini, akan terjadi pemutusan gaya
ion-ion antara Na+ dan Br- dan ikatan hidrogen antara
molekul-molekul air.
4.
Diantara
padatan berikut ini, yang memiliki interaksi antarmolekul hanya melalui gaya
van der Waals adalah
A.
CO2
B.
SiO2
C.
Cu
D.
MgO
E.
CH3CH2OH
Jawab: A
Molekul CO2 adalah
molekul non polar. Molekul non polar hanya memiliki gaya van der Waals.
5.
Jumlah
elektron valensi yang terdapat dalam ion oksalat, C2O42-
adalah:
A.
2
B.
10
C.
32
D.
34
E.
44
Jawab: D
ev C2O42-
= (2 x ev C + 4 x ev O + 2) = (2x4 + 4x6 + 2) = 34
6.
Senyawa
berikut ini, manakah yang mempunyai titik didh paling tinggi?
A.
CH3CH2CH2CH2CH2CH3
B.
CH3CH2OH
C.
CH3CH2CH(OH)CH3
D.
CH3CH2(CH2)2CHO
E.
CH3(CH2)5OH
Jawab: E
Secara sederhana kita
bisa bandingkan titik didih antar zat berdasarkan kepolarannya dan juga panjang
pendeknya rantai
karbon (semakin panjang rantai karbon titik didihnya semakin tinggi), bercabang
atau
lurus (dengan jumlah
atom C yang sama rantai lurus titik didihnya semakin tinggi). Kepolaran alkohol
>
aldehide > alkana
demikian juga titik didihnya, semakin polar maka titik didihnya akan semakin
tinggi,
karena untuk memutus
gaya tarik menarik kutub positif dan negatif antarmolekulnya.
A. CH3CH2CH2CH2CH2CH3
(alkana suku ke–6);
B. CH3CH2OH
(alkohol suku ke–2);
C. CH3CH2CH(OH)CH3
(alkohol skunder suku ke–4);
D. (CH3CH2(CH2)2CHO)Aldehida
suku ke–5;
E. (CH3(CH2)5OH)
alkohol primer suku ke–6
Jadi alternatif E
memiliki titik didih paling tinggi.
7.
Apakah
bentuk molekul IF5?
A.
Oktahedral
B.
Bipiramida
trigonal
C.
Piramida
segiempat
D.
Pyramidal
trigonal
E.
Segiempat
datar
Jawab: C
Notasi AX5E
adalah IF5 yang memiliki bentuk molekul piramida segiempat
8.
Berapa
banyak ikatan sigma dan pi pada senyawa
A.
8
sigma dan 7 pi
B.
11
sigma dan 3 pi
C.
8
sigma dan 3 pi
D.
11
sigma dan 4 pi
E.
10
sigma dan 3 pi
Jawab:
1 Ikatan tunggal = 1 ikatan sigma
1 Ikatan rangkap = 1 ikatan sigma dan 1
ikatan pi
Sehingga jumlah ikatan sigma = 11 dan jumlah
ikatan pi = 3
9.
Ketika
campuran di bawah ini dicampurkan manakah yang akan memisah menjadi 2 lapisan?
A.
Etanol
dan metanol
B.
CCl4
dan metanol
C.
CCl4
dan heksana
D.
Heksana
dan pentana
E.
CCl4
dan pentana
Jawab: B
Kelarutan suatu senyawa ditentukan
berdasarkan prinsip “like disolved like”
yaitu senyawa akan larut dalam senyawa yang sejenis. Senyawa polar larut dalam
senyawa polar dan senyawa nonpolar larut dalam senyawa nonpolar. Dua senyawa
yang tidak sejenis ketika dicampurkan maka akan terbentuk 2 lapisan.
Etanol = polar
Metanol = polar
CCl4 = non polar
Heksana = non polar
Pentana = non polar
Jadi campuran yang membentuk 2 lapisan adalah
campuran antara CCl4 dan metanol.
10.
Satu
dari struktur resonansi ion OCN- yang digambarkan di bawah ini
:Ö̤−C≡N:
:Ö̤−C≡N:
Muatan formal untuk setiap atom dalam
struktur resonansi di atas adalah:
A.
Atom
O = -1, atom C = -1, dan atom N = +1
B.
Atom
O = 0, atom C = 0, dan atom N = -1
C.
Atom
O = -1, atom C = 0, dan atom N = 0
D.
Atom
O = 0, atom C = 0, dan atom N = 0
E.
Atom
O = +1, atom C = 0, dan atom N = -2
Jawab: C
MF O = EV– EB– ½ EI = 6 – 6 – ½ (2) = -1
MF C = EV – EB – ½ EI = 4 – 0 – ½ (8) = 0
MF N = EV – EB – ½ EI =
5 – 2 – ½ (6) = 011. 1. Dari kelompok senyawa berikut ini manakah yang tidak mematuhi aturan oktet?
A.
NH3,
PH3, SO3
B.
H2O,
CH2Cl2, CO2
C.
BF3,
SF4, ICl3
D.
NO2-,
SO32-, SCN-
E.
HOCl,
Cl2CO, N2H4
Jawab: C
Atom B memiliki 6 elektron (tidak mematuhi
aturan oktet)
Atom S memiliki 10 elektron (tidak mematuhi
aturan oktet)
12. Pasangan berikut ini manakah molekul yang memiliki bentuk geometri sama?
A.
AlCl3
dan BCl3 C.
BF3 dan NH3 E.
CO2 dan SO2
B.
AlCl3
dan PCl3 D.
BeCl2 dan H2O
Jawab:
AlCl3 dan BCl3 memiliki geometri molekul yang sama yaitu trigonal planar atau segitiga datar.